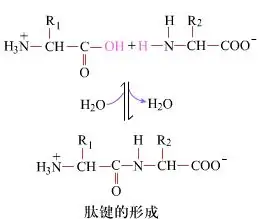
Në sipërfaqe, formimi i lidhjeve peptide, duke prodhuar dipeptide, është një proces i thjeshtë kimik.Kjo do të thotë se dy përbërësit e aminoacideve janë të lidhur nga një lidhje peptide, një lidhje amide, ndërsa janë të dehidratuar.
Formimi i lidhjes peptide është aktivizimi i një aminoacidi në kushte të lehta reagimi.(A) pjesa karboksil, aminoacidi i dytë (B) Pjesa karboksil e aktivizuar nukleofile më pas formon dipeptidin (AB)."Nëse përbërësi karboksil (A) nuk mbrohet, formimi i lidhjes peptide nuk mund të kontrollohet."Nënproduktet si peptidet lineare dhe ciklike mund të përzihen me komponimet e synuara AB.Prandaj, të gjitha grupet funksionale që nuk përfshihen në formimin e lidhjes peptide duhet të mbrohen në një mënyrë përkohësisht të kthyeshme gjatë sintezës peptide.
Pra, sinteza e peptideve - formimi i secilës lidhje peptide - përfshin tre hapa grumbullimi.
Hapi i parë është përgatitja e disa aminoacideve që kanë nevojë për mbrojtje dhe struktura zwitterionike e aminoacideve nuk ekziston më.
Hapi i dytë është një reagim me dy hapa për të formuar lidhje peptide, në të cilën grupi karboksil i aminoacidit të mbrojtur N aktivizohet fillimisht në ndërmjetësin aktiv dhe më pas formohet lidhja peptide.Ky reagim i shoqëruar mund të ndodhë ose si një reagim me një hap ose si dy reaksione të njëpasnjëshme.
Hapi i tretë është heqja selektive ose heqja e plotë e bazës mbrojtëse.Megjithëse e gjithë heqja mund të ndodhë vetëm pasi të jenë mbledhur të gjithë zinxhirët peptidikë, kërkohet gjithashtu heqja selektive e grupeve mbrojtëse për të vazhduar sintezën e peptideve.
Sepse 10 aminoacide (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec dhe Cys) përmbajnë grupe funksionale të zinxhirit anësor, të cilët kërkojnë mbrojtje selektive, duke e bërë sintezën e peptideve më të komplikuar.Bazat mbrojtëse të përkohshme dhe gjysmë të përhershme duhet të dallohen për shkak të kërkesave të ndryshme për selektivitet.Grupet e përkohshme të mbrojtjes përdoren në hapin tjetër për të pasqyruar mbrojtjen e përkohshme të grupeve funksionale të aminoacideve ose karboksileve.Grupet mbrojtëse gjysmë të përhershme hiqen pa ndërhyrë në lidhjet peptide të formuara tashmë ose zinxhirët anësore të aminoacideve, ndonjëherë gjatë sintezës.
“Idealisht, aktivizimi i përbërësit karboksil dhe formimi i mëpasshëm i lidhjeve peptide (reaksionet e çiftëzimit) duhet të jetë i shpejtë, pa formim racemik ose nënprodukt, dhe reaktantët molarë duhet të aplikohen për të arritur rendimente të larta.”Fatkeqësisht, asnjë nga metodat e lidhjes kimike nuk i plotëson këto kërkesa dhe pak janë të përshtatshme për sintezë praktike.
Gjatë sintezës së peptideve, grupet funksionale të përfshira në reaksione të ndryshme zakonisht lidhen me qendrën manuale, përjashtimi i vetëm është glicina dhe ekziston rreziku i mundshëm i rrotullimit.
Hapi i fundit në ciklin e sintezës së peptideve është heqja e të gjitha grupeve mbrojtëse.Heqja selektive e grupeve mbrojtëse është e rëndësishme për shtrirjen e zinxhirit peptid përveç kërkesës për heqjen e plotë të mbrojtjes në sintezën e dipeptideve.Strategjitë sintetike duhet të planifikohen me kujdes.Në varësi të zgjedhjes strategjike, N mund të heqë në mënyrë selektive grupet mbrojtëse α-amino ose karboksil.Termi "strategji" i referohet sekuencës së reaksioneve të kondensimit të aminoacideve individuale.Në përgjithësi, ekziston një ndryshim midis sintezës graduale dhe kondensimit të fragmenteve.Sinteza e peptideve (e njohur edhe si "sinteza konvencionale") zhvillohet në tretësirë.Në shumicën e rasteve, zgjatja graduale e zinxhirit peptid mund të sintetizohet vetëm duke përdorur zinxhirin peptid për të sintetizuar fragmente më të shkurtra.Për të sintetizuar peptide më të gjata, molekulat e synuara duhet të segmentohen në fragmente të përshtatshme dhe të përcaktohen se ato mund të minimizojnë shkallën e diferencimit në fundin C.Pasi fragmentet individuale të grumbullohen gradualisht, përbërja e synuar do të bashkohet.Strategjia e sintezës së peptideve përfshin zgjedhjen e fragmentit mbrojtës më të mirë dhe më të përshtatshëm, dhe strategjia e sintezës së peptideve përfshin zgjedhjen e kombinimit më të përshtatshëm të bazave mbrojtëse dhe metodës më të mirë të konjugimit të fragmenteve.
Koha e postimit: 19-07-2023